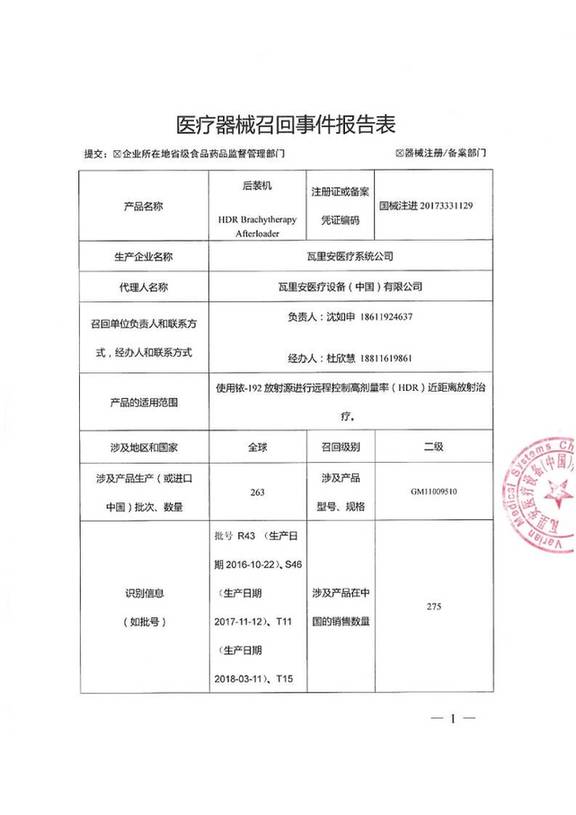
中国质量新闻网讯 据国家药品监督管理局网站2019年8月12日消息,瓦里安医疗系统公司 对其生产的 后装机 HDR Brachytherapy Afterloader(注册或备案号:国械注进20173331129)主动召回。召回级别为 二级 。涉及产品的型号、规格及批次等详细信息见《医疗器械召回事件报告表》。
瓦里安医疗设备(中国)有限公司 报告,瓦里安收到几份报告,称产品部件号为GM11009520的17G不锈钢组织间插植针的尖端断裂。在一个病例中,其中2个插植针尖端被证实留在患者的前列腺内,另外2个插植针尖端治疗后在仪器托盘中找到。该场地咨询泌尿科医师后,决定将2个留在前列腺中的插植针尖端作为位置参考标记,该场地先前就已计划在前列腺中植入位置参考标记,以配合患者治疗。这些尖端没有放射性。目前还没有关于这两个插植针尖端对健康造成不良影响的报告。在咨询泌尿科医师的过程中,延长了患者的麻醉时间。该场地已确认延长麻醉时间不会产生并发症。其他关于插植针尖端断裂的报告,断裂的尖端有的在患者使用前,有的在治疗后清洗过程中被发现。所有报告的断裂的插植针尖端都已说明。受影响部件号为GM11009520和GM11009530,批号为T48和U13,这两个部件号在中国没有销售,因此不采取任何措施,已向国家药品监督管理局和北京市药品监督管理局书面报告了该召回事件。瓦里安近期收到了两起后续报告,批次是 S46 ,在这两起报告中,均在病人治疗前发现了插植针尖端断裂现象(部件号GM11009510 和 GM11009520)。在其中一起报告中,于灭菌后发现插植针尖端弯曲且脱落(部件号GM11009510),尚未收到由于该问题而导致不良健康后果的报告。部件号GM11009510的相关批次在中国有销售,所以需要在中国采取现场措施,召回数量263,其他已销售但尚未发货到客户现场的产品已经隔离并停止发货。